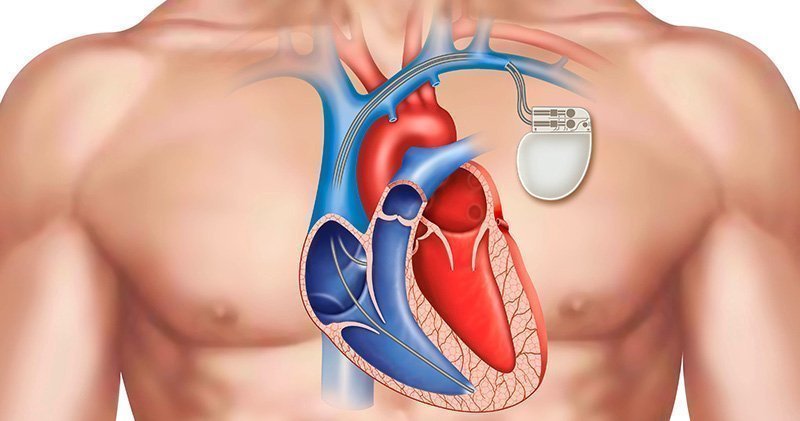
Βηματοδοτικό σύστημα άνευ καλωδίων
Στέφανος Αρχοντάκης, Επικουρικός Επιμελητής Β Καρδιολογίας, Γενικό Νοσοκομείο- Μαιευτήριο ‘’ Έλενα Βενιζέλου’’- Επιστημονικός Συνεργάτης Καρδιολογικής Κλινικής Ιπποκράτειο Γενικό Νοσοκομείο ΑθηνώνΕισαγωγήΣχεδόν 60 χρόνια έχουν περάσει από την ημέρα που το πρώτο επικαρδιακό βηματοδοτικό σύστημα εμφυτεύτηκε σε άνθρωπο από τους Elmquist και Senning στο Νοσοκομείο Karolinska της Στοκχόλμης. Από τότε, σημαντική πρόοδος έχει συντελεστεί στην τεχνολογία των βηματοδοτών, οδηγώντας στα σημερινά πλήρως ενδοκαρδιακά βηματοδοτικά συστήματα που είναι εξαιρετικά αξιόπιστα, χρησιμοποιούν πολύπλοκους αλγόριθμους (δίνοντας έτσι τη δυνατότητα για βηματοδοτική λειτουργία που μιμείται σε μεγάλο βαθμό τη φυσιολογική παραγωγή και διάδοση του ερεθίσματος από το αυτόχθονο ερεθισματαγωγό σύστημα της καρδιάς), είναι μικρότερα σε μέγεθος και διαθέτουν μεγαλύτερης διάρκειας γεννήτριες. Ως αποτέλεσμα αυτών, οι σημερινοί βηματοδότες συνέβαλλαν σημαντικά στην βελτίωση τόσο της πρόγνωσης όσο και της ποιότητας ζωής των ασθενών με βραδυαρρυθμία.
Η εκρηκτική αυτή ανάπτυξη της τεχνολογίας, οδήγησε στη διάδοση των βηματοδοτών και έτσι σήμερα περισσότερες από 700.000 τέτοιες συσκευές εμφυτεύονται ετήσια παγκοσμίως. Σε μια μελέτη που διεξήχθη στον ευρωπαϊκό χώρο το 2011 και συμπεριέλαβε 18 χώρες, ο ετήσιος μέσος ρυθμός εμφύτευσης υπολογίστηκε σε 938 συσκευές ανά εκατομμύριο κατοίκους. Παρόλα αυτά στην Ελλάδα ο ρυθμός εμφύτευσης ήταν σημαντικά χαμηλότερος, στις 629 συσκευές ανά εκατομμύριο κατοίκους, ανά έτος.
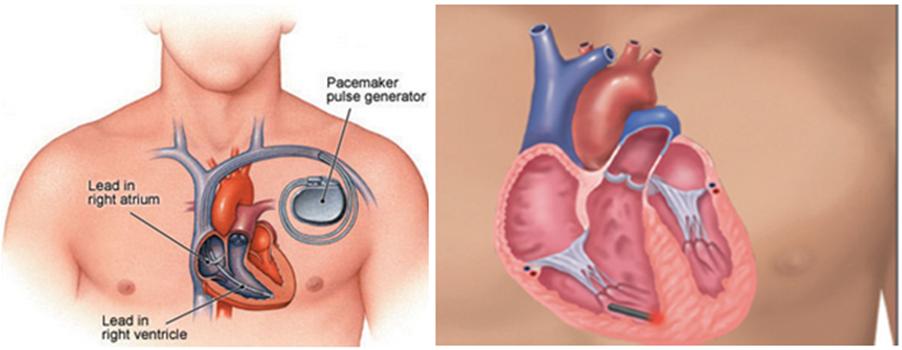
Παρά τη διάδοση των μόνιμων βηματοδότών τα τελευταία χρόνια, η εμφύτευση τους στον ανθρώπινο οργανισμό μπορεί να συνοδεύεται από μια σχετικά μικρή αλλά υπαρκτή πιθανότητα εμφάνισης επιπλοκών, όπως εξάλλου και κάθε άλλη επεμβατική ιατρική πράξη. Οι πιθανές επιπλοκές σχετίζονται κυρίως με την εμφύτευση του διαφλέβιου καλωδίου που συνδέει την βηματοδοτική συσκευή όπου παράγεται το βηματοδοτικό ερέθισμα (η οποία περιλαμβάνει τα ηλεκτρονικά κυκλώματα του βηματοδότη και την μπαταρία του, κλεισμένα σε ένα μεταλλικό κουτί εξαιρετικά στεγανό) με το μυοκάρδιο, πορευόμενο εντός μιας μεγάλης φλέβας. Οι επιπλοκές αυτές μπορεί να συμβούν οξέως κατά την εμφύτευση ή στην περι-επεμβατική περίοδο (πχ πνευμοθώρακας, θραύση η παρεκτόπιση ηλεκτροδίου, τρώση καρδιακού τοιχώματος, επιπωματισμός) ή χρονίως (πχ θρόμβωση ή απόφραξη του φλεβικού δικτύου εντός του οποίου διατρέχει το βηματοδοτικό καλώδιο ή κυριότερα επιμόλυνση του συστήματος, μια δύσκολη και επικίνδυνη για τη ζωή επιπλοκή). Πρόσφατα, ένα μικροσκοπικού μεγέθους, πλήρως εμφυτεύσιμο στη δεξιά κοιλία βηματοδοτικό σύστημα άνευ καλωδίων έχει αναπτυχθεί, εναλλακτικά του παραδοσιακού βηματοδοτικού συστήματος προκειμένου να αντιμετωπιστούν τα παραπάνω προβλήματα.
Χαρακτηριστικά των βηματοδοτών χωρίς καλώδια
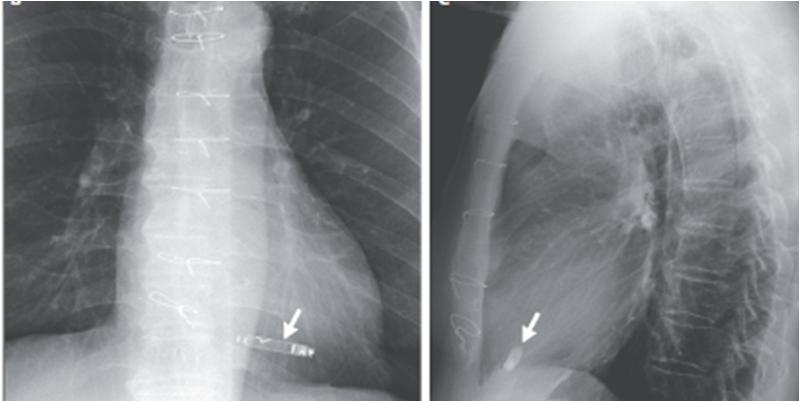
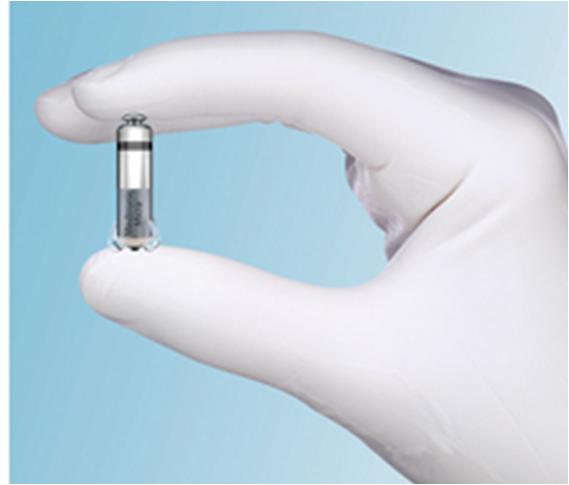
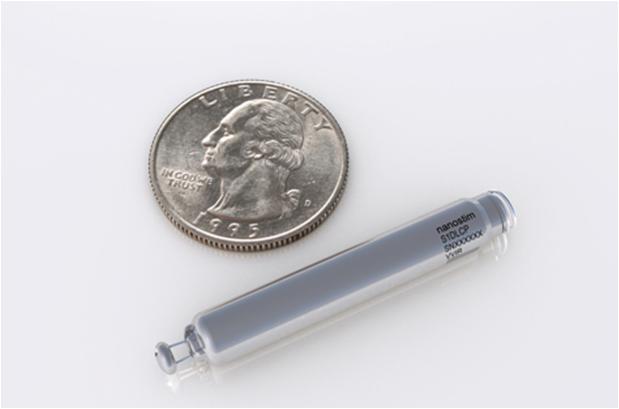
Μέχρι σήμερα, έχουν αναπτυχθεί και χρησιμοποιούνται στην κλινική πράξη δύο τύποι τέτοιων βηματοδοτών χωρίς καλώδια: Το σύστημα Nanostim™ Leadless Pacemaker System (LCP) (St. Jude Medical) και, πιο πρόσφατα, το σύστημα Micra™ Transcatheter Pacing System (TPS) (Medtronic). Οι συσκευές αυτές έχουν σχήμα κάψουλας και είναι σημαντικά μικρότερες συγκριτικά με τους παραδοσιακούς διαφλέβιους βηματοδότες (σημ. για το Nanostim και το Micra: ογκος 1cm3 και διαστάσεις 41.4 x 5.99mm, και όγκος 0.8cm3 και διαστάσεις 25.9 x 6.7mm αντίστοιχα) ενώ ζυγίζουν μόλις 2g. Επί του παρόντος και τα δύο αυτά συστήματα είναι κατάλληλα μόνο για ασθενείς με ένδειξη εμφύτευσης μονοεστιακού βηματοδότη (VVI/VVIR). Οι συσκευές αυτές λειτουργούν με μπαταρίες λιθίου οι οποίες έχουν διάρκεια ζωής 10 περίπου έτη. Ο τρόπος καθήλωσης του βηματοδότη στην καρδιά είναι διαφορετικός στα δύο συστήματα καθώς η συσκευή LCP ‘’βιδώνεται’’ στο μυοκαρδιακό τοίχωμα, ενώ η TPS στερεώνεται στις μυοκαρδιακές δοκίδες του τοιχώματος της δεξιάς κοιλίας μέσω 4 αυτοεκτυσόμενων αγκιστροειδών προσεκβολών από νιτινόλη. Οι συσκευές διαθέτουν δύο ηλεκτρόδια, ένα στο άπω άκρο το οποίο έχει το ρόλο της καθόδου, και στα δυο συστήματα, και ένα δακτυλιοειδές ηλεκτρόδιο (άνοδος) στο μεταλλικό περίβλημα του βηματοδότη σε ότι αφόρα τη συσκευή TPS, ενώ για την LCP το ρόλο της ανόδου τον παίζει η επιφάνεια της συσκευής. Η μακροχρόνια παρακολούθηση και ο προγραμματισμός της συσκευής γίνεται ασύρματα, με τηλεμετρία. Το εγγύς άκρο της συσκευής, τέλος, διαθέτει ένα μηχανισμό που επιτρέπει την επανασύλληψη και απόσυρση του βηματοδότη από το τοίχωμα, σε περίπτωση που χρειαστεί επανατοποθέτηση της συσκευής κατά τη διαδικασία της εμφύτευσης ή αν για οποιοδήποτε λόγο χρειαστεί να αφαιρεθεί η συσκευή. Παρόλα αυτά μέχρι σήμερα δεν υπάρχουν επαρκή στοιχεία σχετικά με την ασφάλεια της αφαίρεσης του συστήματος μεγάλο χρονικό διάστημα μετά απο την εμφύτευση.
Η επέμβαση και στις δύο περιπτώσεις πραγματοποιείται στο εργαστήριο ηλεκτροφυσιολογίας υπό ακτινοσκόπηση, δια της μηριαίας φλέβας με τοπική αναισθησία. Ο βηματοδότης βρίσκεται στην κορυφή ενός ειδικού οδηγού καθετήρα ο οποίος προωθείται υπό ακτινοσκοπική καθοδήγηση διαφλεβίως μέχρι τη δεξιά κοιλία. Το βηματοδοτικό σύστημα παραμένει συνδεδεμένο με τον οδηγό καθετήρα μέχρι να ελεγχθεί η σταθερότητα της θέσης αλλά και να επιβεβαιωθεί η ύπαρξη ικανοποιητικών παραμέτρων αίσθησης της αυτόχθονης ηλεκτρικής δραστηριότητας της καρδιάς και βηματοδότησης από το σύστημα. Μετά την καταγραφή ικανοποιητικών βηματοδοτικών παραμέτρων ακολουθεί η καθήλωση στο μυοκάρδιο. Αν οι παράμετροι βηματοδότησης δεν είναι ικανοποιητικές ο βηματοδότης δύναται να επανατοποθετηθεί σε άλλο σημείο.
Ασφάλεια και αποτελεσματικότητα των βηματοδοτών χωρίς καλώδια
Μετά τα πρώτα ενθαρρυντικά αποτελέσματα σε μελέτες με πειραματόζωα, τα αρχικά δεδομένα των μελετών σε ανθρώπους κατέδειξαν ότι οι βηματοδότες άνευ καλωδίων αποτελούν μια αποτελεσματική και υποσχόμενη θεραπευτική επιλογή για τους ασθενείς που χρήζουν εμφύτευσης μόνιμου βηματοδότη. Η μελέτη LEADLESS υπήρξε μια προοπτική, πολυκεντρική, μη-τυχαιοποιημένη μελέτη η οποία έλαβε χώρα σε 3 ευρωπαικά κέντρα από τον Δεκέμβριο του 2012 μέχρι τον Απρίλιο του 2013, και συμπεριέλαβε 33 ασθενείς στους οποίους εμφυτεύθηκε το σύστημα LCP. Η επιτυχία εμφύτευσης ήταν 97% (n = 32), ενώ η συχνότητα της μη-εμφάνισης επιπλοκών ήταν 94%. Οι παράμετροι βηματοδότησης ήταν συγκρίσιμες με αυτές που καταγράφονται στους κλασικούς βηματοδότες και παρέμειναν αμετάβλητες κατά τη μακροχρόνια παρακολούθηση.
Μετά την δημοσίευση της πρωτοποριακής αυτής μελέτης, η αποτελεσματικότητα και η ασφάλεια των συσκευών αυτών επιβεβαιώθηκε και σε δύο μεγαλύτερες, προοπτικές, μη-τυχαιοποιημένες, πολυκεντρικές μελέτες, τη μελέτη LEADLESS II trial που χρησιμοποίησε το σύστημα Nanostim™ Leadless Pacemaker System (LCP) και τη μελέτη Micra Transcatheter Pacing System (Micra-TPS) που μελέτησε το σύστημα Micra™ Transcatheter Pacing System (TPS).
Η LEADLESS II συμπεριέλαβε 526 ασθενείς που εντάχθηκαν στη μελέτη μεταξύ Φεβρουαρίου 2014 και Ιουνίου 2015 σε 56 κέντρα σε 3 χώρες. Οι 300 από τους ασθενείς αυτούς είχαν ήδη συμπληρώσει 6μηνη παρακολούθηση μετά την εμφύτευση όταν δημοσιεύτηκαν τα αποτελέσματα της μελέτης. Η συσκευή εμφυτεύτηκε επιτυχώς στο 95.8% των ασθενών και ο μέσος χρόνος όλης της διαδικασίας εμφύτευσης ήταν 50 λεπτά. Η αποτελεσματική λειτουργία του βηματοδότη επιβεβαιώθηκε στο 93.4% των ασθενών στους οποίους η συσκευή εμφυτεύτηκε επιτυχώς και είχαν συμπληρώσει την 6μηνη παρακολούθηση. Επιπλέον στο 93.3% των ασθενών δεν παρατηρήθηκαν αξιόλογες επιπλοκές. Επιπλοκές παρατηρήθηκαν στο 6.7% των ασθενών, οι κυριότερες από τις οποίες ήταν η εκτόπιση της συσκευής από την αρχικά εμφυτευθείσα θέση (1.7%), η τρώση του καρδιακού τοιχώματος (1.3%) και η απώλεια των ικανοποιητικών βηματοδοτικών παραμέτρων (1.3%). Τέλος, δεν καταγράφηκε κανένας θάνατος σχετιζόμενος με την συσκευή. Η μελέτη Micra-TPS συμπεριέλαβε 725 ασθενείς που εντάχθηκαν στη μελέτη σε 56 κέντρα σε 19 χώρες. Οι 297 από τους ασθενείς αυτούς είχαν ήδη συμπληρώσει 6μηνη παρακολούθηση μετά την εμφύτευση όταν δημοσιεύτηκαν τα αποτελέσματα της μελέτης. Ο βηματοδότης έγινε δυνατό να εμφυτευθεί στο 99.2% των περιπτώσεων (719 από τους 725 ασθενείς) και η αποτελεσματική λειτουργία του βηματοδότη επιβεβαιώθηκε στο 98.3% των ασθενών στους οποίους η συσκευή εμφυτεύτηκε επιτυχώς και είχαν συμπληρώσει την 6μηνη παρακολούθηση. Η εμφύτευση ήταν ανεπίπλεκτη στο 96% των περιπτώσεων. Οι κυριότερες επιπλοκές που καταγράφηκαν ήταν η τρώση του καρδιακού τοιχώματος (1.6%) και τοπικές επιπλοκές στο σημείο παρακέντησης στο μηρό (0.7%). Δεν καταγράφηκε παρεκτόπιση από το σημείο αρχικής εμφύτευσης ούτε κάποιος θάνατος σχετιζόμενος με την συσκευή.
Τα αποτελέσματα και στις δύο μελέτες είναι συγκρίσιμα με αυτά από των εμφυτεύσεων των κλασικών βηματοδοτών και καταδεικνύουν την ασφάλεια και την αποτελεσματικότητα της χρήσης των συστημάτων αυτών.
Δυνητικά οφέλη και μειονεκτήματα
Το βασικό πλεονέκτημα της νέας αυτής τεχνολογίας αποτελεί η εξάλειψη των βηματοδοτικών καλωδίων και των πιθανών επιπλοκών που σχετίζονται με αυτά, οξέων ή χρόνιων. Επιπλέον σε άτομα που η εμφύτευση είναι εργώδης λόγω δύσκολης πρόσβασης από το αγγειακό δίκτυο της Άνω Κοίλης Φλέβας, η διαδικασία απλοποιείται. Ακόμα, από αισθητικής πλευράς είναι προτιμητέα, αφού αποφεύγεται η ύπαρξη της κλασικής ουλής, στην περιοχή κάτω από την κλείδα. Τέλος, η διάρκεια ζωής της γεννήτριας μπορεί, με τις κατάλληλες ρυθμίσεις, να είναι μεγαλύτερη από αυτή στους συμβατικούς βηματοδότες (μεγαλύτερη από 10 έτη!), ενώ οι ασθενείς με τις συσκευές αυτές μπορούν να υποβληθούν σε Μαγνητική Τομογραφία στο θώρακα.
Στα μειονεκτήματα των βηματοδοτών χωρίς καλώδια συγκαταλέγονται, το γεγονός ότι δεν είναι δόκιμο να χρησιμοποιηθούν σε όλους τους ασθενείς με βραδυαρρυθμία αλλά μόνο επί συγκεκριμένων ενδείξεων, το γεγονός ότι παρά το ότι οι πρώτες, προαναφερθείσες, μελέτες έδειξαν ενθαρρυντικά αποτελέσματα σίγουρα θα χρειαστούν περισσότερες και μεγαλύτερες μελέτες προκειμένου η θέση των συσκευών αυτών να εδραιωθεί στην κλινική πράξη, και βέβαια το υψηλότερο κόστος. Τέλος, δεν είναι γνωστό ακόμα αν η καλύτερη τακτική σε περίπτωση εξάντλησης της μπαταρίας θα ήταν η αφαίρεση του βηματοδότη ή η εμφύτευση ενός καινούργιου αφήνοντας τον παλιό στη θέση του, αν και φαίνεται ότι προάγεται μάλλον η δεύτερη λύση. Ακόμα και τότε όμως δεν είναι ακόμα γνωστό ποιο είναι το αριθμητικό όριο των συσκευών που μπορεί να εμφυτευθούν στον περιορισμένο χώρο της δεξιάς κοιλίας.
Συμπέρασμα
Μπορεί επομένως να ειπωθεί, με βάση τα παραπάνω, ότι η εμφάνιση των βηματοδοτών χωρίς καλώδια ανοίγει μια νέα εποχή στον τομέα της βηματοδότησης. Παρά τα πρώτα ενθαρρυντικά αποτελέσματα, παρόλα αυτά, θα χρειαστούν και νέες μελέτες που θα εξετάσουν την ασφάλεια και την αποτελεσματικότητα της τεχνολογίας αυτής, ενώ περεταίρω βελτιώσεις, κυρίως ως προς τη δυνατότητα βηματοδότησης περισσότερων από μιας καρδιακών κοιλοτήτων διαδοχικά ή τη συνεργασία με άλλες συσκευές όπως τους υποδόριους απινιδωτές είναι απαραίτητες προκειμένου να διαδοθούν οι συσκευές αυτές ευρέως.
Η ανάπτυξη τα τελευταία χρόνια πολλών και δαπανηρών νέων τεχνολογιών στην ιατρική υποχρεώνει εκ των πραγμάτων τα συστήματα υγείας στο να θεσπίσουν συγκεκριμένες ενδείξεις για τη χρήση αυτών, κάτι που ισχύει ασφαλώς και για την Ελλάδα, λόγω των περιορισμένων διαθέσιμων πόρων για την υγεία. Παρόλα αυτά, οι νέοι βηματοδότες χωρίς καλώδια έχουν θέση, υπό την προϋπόθεση ότι γίνεται ορθολογική και εξατομικευμένη χρήση τους κυρίως σε ασθενείς που δεν υπάρχει η τεχνική δυνατότητα για την εμφύτευση συμβατικού βηματοδότη, και επομένως οι νέες συσκευές θα αποτελούσαν τη μόνη εναλλακτική λύση.
REFERENCES
Mond HG, Proclemer A. The 11th world survey of cardiac pacing and implantable cardioverter-defibrillators: calendar year 2009—a World Society of Arrhythmia’s project. Pacing Clin Electrophysiol 2011; 348: 1013- 1027.
Brignole M, Auricchio A, Baron-Esquivias G, et al. 2013 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. Addenda. Tthe Task Force on cardiac pacing and resynchronization therapy of the European Society of Cardiology (ESC). Developed in collaboration with the European Heart Rhythm Association (EHRA). Eur Heart J 2013; 34:2281-329.Sperzel J, Burri H, Gras D, et al. State of the art of leadless pacing. Europace 2015; 17:1508-13.
Echt DS, Cowan MW, Riley RE, Brisken AF. Feasibility and safety of a novel technology for pacing without leads. Heart Rhythm 2006;3:1202–6.
Lee KL, Lau CP, Tse HF, et al. First human demonstration of cardiac stimulation with transcutaneous ultrasound energy delivery: implications for wireless pacing with implantable devices. J Am Coll Cardiol 2007;50:877–83.
Miller MA, Neuzil P, Dukkipati SR, Reddy VY. Leadless Cardiac Pacemakers: Back to the Future. J Am Coll Cardiol 2015; 66:1179-89.
Auricchio A, Delnoy PP, Butter C, et al. Feasibility, safety, and short-term outcome of leadless ultrasound-based endocardial left ventricular resynchronization in heart failure patients: results of the Wireless Stimulation Endocardially for CRT (WiSE-CRT) study. Europace 2014;16:681–8.